INSTITUCIÓN EDUCATIVA INEM – JOSE CELESTINO MUTIS
RECUPERACIONES - QUÍMICA
IV PERIODO - DENSIDAD
1. Consulte la forma en la que se puede calcular la densidad del agua por medio de una probeta y por medio de un picnómetro.
2. Realice un dibujo de los materiales de laboratorio necesarios para calcular la densidad de un líquido.
3. Sustente el por qué la densidad del agua pura es diferente a la densidad del agua de mar.

INSTITUCIÓN EDUCATIVA INEM – JOSE CELESTINO MUTIS
RECUPERACIONES QUÍMICA
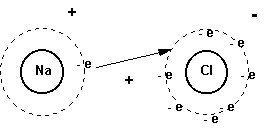
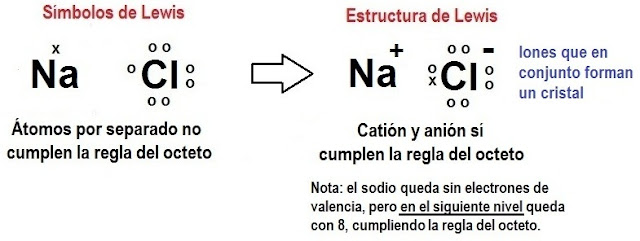
III PERIODO – ENLACES QUÍMICOS
Conteste las
preguntas 1 y 2 de acuerdo a la información de la siguiente tabla:
La tabla presenta la electronegatividad de 4 elementos X, J, Y y L
Elemento
|
X
|
J
|
Y
|
L
|
Electronegatividad
|
4.0
|
1.5
|
0.9
|
1.6
|
1. De acuerdo con la información de la tabla, es válido afirmar que el
compuesto con mayor carácter iónico es, sustente su respuesta.
A. LX
B. JL
C. YJ
D. YX
2. De acuerdo con la
información de la tabla, es válido afirmar que el compuesto de mayor carácter
covalente es, sustente su respuesta.
A. LY
B. JL
C. YX
D. YJ
3. Teniendo en cuenta
que los valores de la electronegatividad de los siguientes elementos: H: 2,1 ; O: 3,5 ; Na: 0,9 ; S: 2,5 y Cl: 3,0 ¿Cuál de
los siguientes enlaces es más polar? Sustente
su respuesta.
A. HO
B. HNa
C. HS
D. HCl
D. HCl
4. En las reacciones
químicas, las partículas de los átomos que interactúan para producir nuevas
sustancias son
A. los electrones que
hay en el núcleo.
B. los protones del
último nivel de energía.
C. los neutrones de
los orbitales enlazados.
D. los electrones de
valencia.
5. ¿En cuál de los
compuestos siguientes tiene un enlace fundamentalmente iónico? Sustente su respuesta.
A. H2O
B. CCl4
C. BeH2
D. NaI
6. Teniendo en cuenta la electronegatividad de
los elementos, en cuanto al tipo de enlace que se formará entre los elementos
que se indican, seleccione la respuesta correcta.
A. El Ca y el O forman un enlace covalente
polar
B. El H y el Cl forman un enlace iónico
C. El K y el F forman un enlace iónico
D. El H y en Br forman un enlace covalente
apolar
7. Indica cuál de los
siguientes compuestos es iónico y demuéstrelo por medio de su
electronegatividad, distribución electrónica, modelo atómico, Lewis y enlaces
químicos.
A. HCl
B. NaBr
C. CS2
D. N2O
D. N2O
8. La representación de Lewis que mejor corresponde al
nitrógeno, N2, ubicado en el grupo VA de la tabla periódica, es:
Conteste las preguntas 9 de
acuerdo con la siguiente tabla
10. demuestre
por medio de la electronegatividad, distribución
electrónica, modelo atómico, Lewis y enlaces químicos, cuál pareja de elementos se une por medio de un enlace covalente
polar o apolar.
A. Plata y oxígeno
B. Potasio e hidrógeno
C. Hidrógeno y azufre
D. Sodio y Cloro
D. Sodio y Cloro
INSTITUCIÓN EDUCATIVA INEM JOSE CELESTINO MUTIS
RECUPERACIÓN DE QUÍMICA
II PERIODO – GRADO ° 7
1. En la siguiente tabla periódica ubique los siguientes grupos:
a. Alcalinos
b. Alcalinotérreos
c. Gases nobles
d. Metaloides
e. No metales
f. Metales
2. Realice el triángulo de Mouller y explique para que
puede ser utilizado en su clase de química.
3. Teniendo en cuenta el triángulo de Mouller,
realice las distribuciones electrónicas para los siguientes elementos. Tenga en
cuenta elaborar los modelos atómicos y las estructuras de Lewis.
Mg – Co – Se – Sr - Xe
4. Con base en toda la información adquirida en este periodo, identifique
el periodo y el grupo al que pertenece cada uno de los siguientes elementos
químicos, teniendo como base su distribución electrónica. Además, debe elaborar
el modelo atómico y la estructura de Lewis.
Fr – P – Sn – Cs